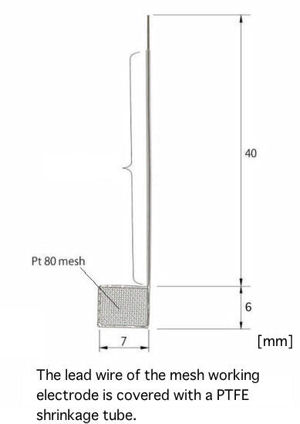
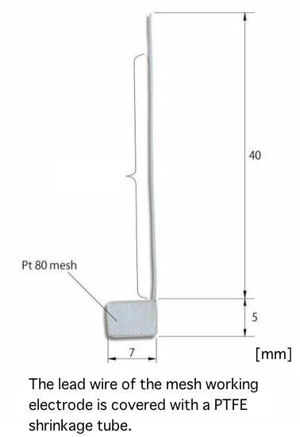
"Tipos de células espectroelectroquímicas"
Para las células espectroelectroquímicas, existe un tipo de célula de lote y un tipo de célula de flujo.
Tipo de célula de lote utilizando un electrodo de malla de platino o de oro como electrodo de trabajo. Tipo de célula de flujo usando una retícula de platino, oro y carbono, y electrodos ITO como electrodo de trabajo.
La espectroelectroquímica (SEC) está dirigida a la investigación del mecanismo de reacción electroquímica y la estructura de la interfase entre la solución electrolítica y el electrodo. Los progresos notables en este campo y la tecnología relacionada permiten que la SEC se aplique en áreas amplias.
En la actualidad, la relación entre la absorbancia y el potencial para el sistema reversible o cuasi-reversible es teóricamente elucidado, sobre cuya base el análisis de las características electroquímicas se hace posible para el sistema de otra manera difícil con sólo el resultado del voltamograma.
Un ejemplo típico es la enzima redox citocromo c y el azul de metileno.
- Dos variedades longitud de la trayectoria óptica (0.5 y 1.0 mm)
- Diseñado para utilizar el electrodo de referencia de 6,0 mm
- Dos variedades de electrodos de trabajo (Au o Pt)
- Ser capaz de utilizar en un espectrómetro estándar
Comparación de 0,5 y 1,0 células de longitud de trayectoria óptica
El tiempo de estabilización de la electrólisis para la célula de longitud de trayectoria óptica de 0,5 mm es teóricamente la mitad, en comparación con la celda de 1,0 mm. Es lo opuesto, para la concentración, cuando es posible el mismo resultado para la celda de 1,0 mm para una mitad de la concentración en comparación con la celda de 0,5 mm. Puede seleccionar la longitud de la trayectoria óptica y el electrodo de trabajo adecuado para su propósito de investigación.
| Longitud de la trayectoria óptica |
Mérito |
Desmérito |
| 0,5 mm |
Alta velocidad electrolítica |
Mantenimiento difícil |
| 1,0 mm |
Facil mantenimiento |
Velocidad electrolítica lenta |
Comparación del tiempo de equilibrio de la reacción de electrólisis
Para la comparación de las células de longitud de trayectoria óptica de 0,5 y 1,0, existe una diferencia entre los valores teóricos y experimentales. Es en consecuencia de las condiciones experimentales.
| Fig.1-1. Absorbancia para la electrólisis realizada con una celda de longitud de trayectoria óptica de 0,5 mm |
|
Fig.1-2. Absorbancia para electrólisis realizada con celda de longitud de trayectoria óptica de 1,0 mm |
  |
|
  |
|
Se sometió un ferrocianuro de potasio 2 mM (K4 [Fe (CN) 6 ]) a una reacción de electrólisis a 0,6 V hasta su estabilidad, y se utilizó KNO3 1 M como referencia. La reacción de oxidación se controló mediante la comparación de la absorbancia en función del tiempo a longitudes de onda de 420 y 300 nm.
Longitud del trayecto óptico 1,0 mm
La longitud de la trayectoria óptica de 1,0 mm es la más adecuada para las mediciones básicas de electroquímica de espectro. Teóricamente, es posible obtener el mismo resultado que para 0,5 mm con una muestra de la mitad de la concentración.
| Nº de catálogo |
Descripción |
| 013510 |
Kit de celda de espectroelectroquímico de capa fina de vidrio de cuarzo (Pt) SEC-C |
| 013511 |
Kit de celda de espectroelectroquímico de capa fina de vidrio de cuarzo (Au) SEC-C |
| Componentes comunes |
| 012906 |
Contra electrodo de platino SEC-C |
| 013512 |
Célula de vidrio de cuarzo de capa delgada SEC-C |
| 011501 |
Tapa de teflón SEC-C |
| (010537) |
Tubo de purga de 10 cm |
| Electrodos de trabajo |
| 011498 |
Electrodo de trabajo de gasa de platino SEC-C |
| 012017 |
Electrodo de trabajo de gasa de oro SEC-C |
| Productos opcionales |
| 012167 |
RE-1B Electrodo de referencia (Ag / AgCl) |
| 012171 |
RE-7 Electrodo de referencia no acuoso (Ag / Ag + ) |
Longitud del trayecto óptico 0,5 mm
La longitud de la trayectoria óptica 0,5 mm tiene un tiempo de electrólisis más corto que una celda de 1,0 mm. El tiempo de estabilidad breve para la electrólisis hace posible tener un resultado estable como para, la medición del disolvente orgánico de alta volatilidad, la detección de los productos de electrólisis inestables, y otros.
* Hay un electrodo de trabajo específico para la longitud del camino óptico de 0.5 mm. El electrodo de trabajo para una longitud de trayectoria óptica de 1,0 mm no se puede utilizar en celdas de cuarzo de longitud óptica de 0,5 mm.
| Nº de catálogo |
Descripción |
| 012813 |
Kit de células espectroelectroquímicas de vidrio de cuarzo de capa delgada (Pt) SEC-C05 |
| 012814 |
Kit de células espectroelectroquímicas de vidrio de cuarzo de capa delgada (Au) SEC-C05 |
| Componentes comunes |
| 012609 |
Contra electrodo de platino SEC-C05 |
| 012815 |
Célula de cristal de cuarzo de capa delgada SEC-C05 |
| 011501 |
Tapa de teflón SEC-C |
| (010537) |
Tubo de purga de 10 cm |
| Electrodos de trabajo |
| 012606 |
Electrodo de trabajo de gasa de platino SEC-C05 |
| 012607 |
Electrodo de trabajo de gasa de oro SEC-C05 |
| Productos opcionales |
| 012167 |
RE-1B Electrodo de referencia (Ag / AgCl) |
| 012171 |
RE-7 Electrodo de referencia no acuoso (Ag / Ag + ) |
Ejemplo de medición utilizando células espectroelétroquímicas tipo cuvetas
Se midieron el espectro de absorción UV-visible y la absorbancia del producto de la reacción de electrodo, realizada con electrodo ópticamente transparente (OTE). Se utilizó electrodo de malla de oro o platino como OTE. La voltamperometría cíclica y la absorbancia del ferricianuro de potasio 2 mM, como referencia de la absorbancia, realizada en una celda especetroelectroquímica de vidrio de cuarzo de capa delgada SEC-C se muestran a continuación (Figura 2-1, 2-2).
  |
|
  |
| Fig.2-1. Voltamperometría cíclica para ferricianuro de potasio 2 mM. |
|
Fig.2-2. Espectro de absorción del balance electrolítico para ferricianuro de potasio 2 mM electrolizado a diferentes potenciales. |
También se realizaron mediciones simultáneas de la voltametría cíclica y absorbancia, así como una medición de la electrólisis potencial constante. A continuación se muestra la electrólisis, la reducción (Figura 3-1) y la oxidación (Figura 3-2) de la solución de ferrocianuro de potasio.
  |
|
  |
| Fig.3-1. Cambios de absorbancia para la reducción del ferrocianuro de potasio. |
|
Fig.3-2. Cambios de absorbancia para la oxidación del ferricianuro de potasio. |
|